



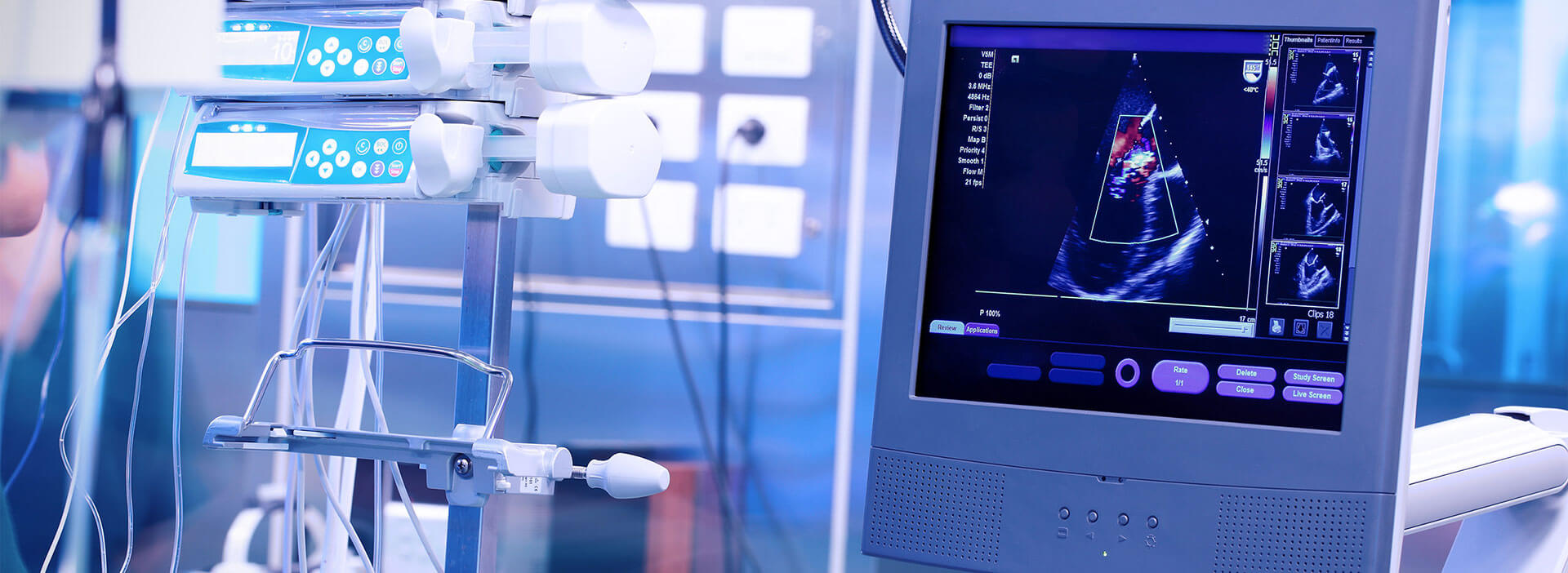
De ISO 13485-standaard is een zeer effectieve oplossing die is ontwikkeld voor bedrijven die medische apparaten produceren die voldoen aan de vereisten van een kwaliteitsbeheersysteem. De publicatie van de ISO 13485 Medical Devices Quality Management System-standaard heeft een belangrijke leemte opgevuld voor fabrikanten en leveranciers om te werken in overeenstemming met de richtlijnen voor medische hulpmiddelen en de nationale wettelijke voorschriften die in de landen van de Europese Unie worden gepubliceerd, evenals om hun verantwoordelijkheden na te komen en verplichtingen na te komen ten aanzien van de veiligheid en kwaliteit van medische apparaten. .
ISO 13485-norm is 's werelds meest populaire en meest gebruikte standaard voor kwaliteitsbeheer van medische apparaten. Oorspronkelijk ontwikkeld door de International Standards Organization (ISO) in 2003, werd deze standaard voor het laatst herzien in 2016. De huidige versie is ISO 13485: 2016.
De ISO 13485-standaard, die wereldwijd wordt geaccepteerd, is een onafhankelijke managementsysteemstandaard die is gebaseerd op ISO 9000 Quality Management System-norm. Daarom zijn de processen van dit systeem gebaseerd op de plannings-, uitvoerings-, besturings- en voorzorgcyclus en vereisen dat de processen worden ontworpen in overeenstemming met de geldende wettelijke voorschriften. De ISO 13485-standaard is zeer beschrijvend en ondersteunt fabrikanten van medische apparaten. De standaard heeft als doel veilige medische apparaten te ontwerpen, ontwikkelen, produceren, leveren en installeren.
Allerlei fabrikanten van medische apparaten, of ze nu lokaal willen uitbreiden of internationaal willen concurreren, kunnen ISO 13485 Medical Devices Quality Management System Certificate verkrijgen. Met dit document verhogen ondernemingen hun prestaties, elimineren ze onzekerheden in processen en streven ze gemakkelijker naar marktkansen. Maar het belangrijkste is dat deze bedrijven zich inzetten voor kwaliteit aan de ene kant voor hun klanten en officiële instellingen.
De voordelen van ISO 13485 Medical Devices Quality Management System Certificate kunnen als volgt worden vermeld:
Bedrijven kunnen meer markten bereiken en op de wereldmarkten concurreren
De processen in het bedrijf worden beoordeeld en herbekeken met de kwaliteitsaanpak
De productiviteit stijgt, de kosten dalen en de prestaties van de supply chain verbeteren
Veiliger en effectievere medische hulpmiddelen worden geproduceerd
Verantwoordelijkheden die voortvloeien uit wettelijke voorschriften zijn vervuld
Aan de eisen en verwachtingen van de klant wordt voldaan
ISO 13485 Medical Devices Quality Management System is het beste internationaal erkende model dat door een bedrijf in medische hulpmiddelen kan worden toegepast om naleving van wet- en regelgeving in de sector medische hulpmiddelen te ondersteunen. Deze norm is een norm voor kwaliteitsmanagementsysteem die wordt aanvaard als de basis van medische hulpmiddelen met CE-markering volgens de richtlijnen die gelden in de landen van de Europese Unie. Tegenwoordig is de ISO 13485-norm wereldwijd nodig in de industrie voor medische apparatuur.
In feite is het ISO 13485-certificaat geen absolute vereiste voor CE-gemarkeerde medische apparaten volgens de Europese richtlijnen voor medische hulpmiddelen. Niettemin wordt het door de Europese Commissie als een geharmoniseerde norm geaccepteerd.
ISO 13485: 2016 februari 28 heeft een overgangsperiode gekregen voor fabrikanten van medische apparaten om te upgraden naar 2019. Om de huidige ISO 13485-documentatie te behouden, moeten fabrikanten vóór deze datum voldoen aan de vereisten van de ISO 13485: 2016-versie. Deze nieuwste versie voldoet aan de richtlijnen voor medische hulpmiddelen van de Europese Unie. Standaardharmonisatie stelt fabrikanten in staat om hun naleving van de norm te gebruiken als bewijs van naleving van de vereisten van de relevante wettelijke voorschriften. Bedrijven die medische hulpmiddelen naar landen in de Europese Unie zullen sturen, zullen worden geëvalueerd volgens de EN ISO 1: 2019-versie vanaf april 13485-datum.
EN ISO 13485: De harmonisatie van de 2016-standaard is een belangrijke stap in de richtlijn hulpmiddelen voor in-vitrodiagnostiek, die de bestaande richtlijnen zal vervangen.
Het ISO 13485 Medical Devices Quality Management System heeft tot doel ervoor te zorgen dat organisaties in de sector medische hulpmiddelen een internationaal erkende standaard hebben. Het systeem stemt de vereisten voor de productie van medische apparaten voornamelijk af op systemen voor kwaliteitsborging. In dit systeem, dat in één keer algemeen wordt geaccepteerd, werd het 2015-document wereldwijd in 26255 uitgegeven.
Kortom, ISO 13485-certificaat bewijst dat de bedrijven die actief zijn in de sector medische apparaten een kwaliteitsmanagementsysteem toepassen dat voldoet aan de norm. Deze benadering omvat niet alleen fabrikanten van medische hulpmiddelen, maar ook leveranciers, bedrijfsvertegenwoordigers en adviesbureaus die op dit gebied werkzaam zijn. Naarmate de ISO 13485-standaard wordt ontwikkeld, breiden de profielen van bedrijven en organisaties die deze standaard kunnen implementeren zich uit. Quality Management System is een levend systeem. De veranderingen en ontwikkelingen die van invloed zijn op de markten worden bewaakt en zij ondersteunen de regulering en versterking van de processen en procedures in de onderneming.
Hierboven is vermeld dat de ISO 13485-norm gericht is op de harmonisatie van kwaliteitsmanagementsystemen binnen het kader van de vereisten voor het ontwerpen, ontwikkelen, produceren en installeren van medische apparaten. Tegenwoordig zijn veel overheidsinstanties op zoek naar en zelfs een ISO 13485-certificaat van fabrikanten van medische apparaten. In het buitenland vereisen regelgevende instanties een ISO 13485-certificaat als onderdeel van hun vereisten om de verkoop van medische hulpmiddelen in hun thuisland te garanderen.
Canada vereist bijvoorbeeld dat fabrikanten ISO 13485-certificering verkrijgen voor marktgoedkeuring voor bepaalde medische apparaten. Bovendien moeten bedrijven een erkend certificeringsbedrijf alleen selecteren in overeenstemming met de Canadese regelgeving om dit certificaat te verkrijgen.
Over het algemeen is de naleving van ISO 13485 Medical Devices Quality Management System vrijwillig een beheersysteem dat fabrikanten moeten implementeren om internationale markten te bereiken. Het hebben van het ISO 13485-certificaat geeft de bedrijfspartners het vertrouwen dat het bedrijf ernaar streeft om aan de norm te voldoen.
De vereisten van deze internationale norm kunnen ook worden gebruikt voor het vervaardigen of bedienen van externe leveranciers, zoals grondstoffen, componenten, subassemblages, geneesmiddelen, sterilisatiematerialen, kalibratiediensten, distributiediensten en onderhoudsdiensten. Leveranciers of andere externe bedrijven kunnen vrijwillig overeenkomen om te voldoen aan de vereisten van de ISO 13485-standaard of kunnen door de fabrikant worden verplicht hieraan te voldoen. Als gevolg daarvan vereist de norm dat bedrijven voldoen aan de vereisten van de relevante wettelijke voorschriften.
Eerst wordt bepaald of de organisatie voldoet aan de verplichte eisen van de norm en of naar de volgende fase moet worden gegaan.
Er wordt gecontroleerd of noodzakelijke procedures en audits zijn ontwikkeld en of de bereidheid van uw instelling tot evaluatie is beoordeeld.
De bevindingen die in de eerste twee fasen optreden, worden geëvalueerd en nadat corrigerende acties zijn beoordeeld, wordt de documentvoorbereiding gestart.
U kunt ons vragen om ons formulier in te vullen om een afspraak te maken, voor meer gedetailleerde informatie of om een evaluatie aan te vragen.